本連載が、『疫学 新型コロナ論文で学ぶ基礎と応用』と題して、単行本になります。ぜひお手にとってご覧ください。
 世界的な業績のある疫学者が、新型コロナ論文を題材に疫学の基礎から応用をわかりやすく解説。基本用語から最先端技法まで網羅する!
世界的な業績のある疫学者が、新型コロナ論文を題材に疫学の基礎から応用をわかりやすく解説。基本用語から最先端技法まで網羅する!
※「まえがき」と「あとがき」をたちよみできます。⇒【たちよみはこちら】
2021年12月22日発売
坪野吉孝 著 『疫学 新型コロナ論文で学ぶ基礎と応用』
A5判並製・240頁 本体価格2700円(税込2970円)
ISBN:978-4-326-70121-6 →[書誌情報]
【内容紹介】 ランダム化比較対照試験、前向きコホート研究、症例対照研究など、疫学で使われる研究デザインとは? 世界を代表する医学専門誌に掲載された新型コロナ論文を読み解きながら、疫学の考え方を非医療者も理解できるようわかりやすく解説する。データと論理と知性の力によって無数の人々の生命を救う、疫学の成果と課題を知るために。
2020年、世界中で新型コロナウイルスのパンデミックが進行するさなか、英国ではその治療薬を探す臨床試験が大規模に行われていました。従来の発想では考えられない取り組みの結果、身近な薬の効果がきわめて短期間に探り当てられた背景を、疫学論文から読み解きます。[編集部]
Covid-19が猛威をふるい、世界で多数の感染者が出ていた2020年当初、入院した患者の死亡を防げる治療法はなかった。インフルエンザに対するタミフルなどのような、新型コロナウイルスに特異的にはたらく治療薬は、むろんまた開発されていない。すでに存在する薬物のなかから、Covid-19に効果を発揮する薬物を探す、暗中模索がはじまった。
Covid-19による入院患者の死亡リスクを改善する効果が、さいしょにしっかりと確認されたのは、副腎皮質ホルモンの一種であるデキサメタゾンだ。デキサメタゾンは、世界のどこの病院にも置いてあるような、きわめてありふれた薬剤である。日本の薬価は、ジェネリック錠剤1錠(4mg)が、わずか29.9円。点滴や注射に使う1アンプル(6.6mg)が、たったの149円しかしない。
ありふれて安価なこのデキサメタゾンだが、Covid-19入院患者の死亡を減らす効果の有無を調べた研究は、ランダム化比較対照試験(RCT)の方法で行われた。それも、「臨床試験の教科書を書き換える」と評されるような革新的な方法が使われた。
https://www.thelancet.com/journals/landig/article/PIIS2589-7500(21)00063-7/fulltext
この臨床試験のプロジェクトは、「RECOVERY Trial」と名付けられた。”RECOVERY“は、Randomised Evaluation of COVID-19 Therapyという、研究プロジェクトの正式名称の頭文字などを取った略称。この略称に、recoveryの「回復」という意味がかけ合されている。こうした語呂合わせのような命名もよくある。WHOが国際協同で組織したCovid-19患者の治療薬の臨床試験の名前は、「SOLIDARITY Trial」。Solidarityつまり「連帯」をもじった命名だった。
RECOVERY試験は、英国オックスフォード大学が組織した。英国の176施設が参加し、同国のCovid-19入院患者の約10%が登録された。デキサメタゾン、抗マラリア薬のヒドロキシクロロン、抗HIV薬のロピナビル・リトナビル合剤、抗菌薬のアジスロマイシンなど、ほかの疾患の治療薬としてすでに存在するさまざまな薬剤の、Covid-19入院患者に対する有効性と安全性を、つぎつぎと評価するように研究計画が立てられた。ひとつの臨床試験プロジェクトのなかで、複数の薬剤の有効性と安全性を、同時進行で評価した。
デキサメタゾンに関する部分の論文は、暫定的な報告が2020年7月17日に『ニュー・イングランド・ジャーナル・オブ・メディスン』(NEJM)にオンライン公開され、内容を改定した最終報告が2021年2月25日に印刷版で出版された。日本語抄録も公開されている。最終報告版の論文の抄録に補足を加えながら、研究のあらましを見てみよう。
https://www.nejm.org/doi/full/10.1056/NEJMoa2021436
https://www.nejm.jp/abstract/vol384.p693
背景: デキサメタゾンのような糖質コルチコイド(副腎皮質ホルモンの一種)は、炎症を抑えることで、Covid-19による肺の損傷の悪化を防ぎ、呼吸不全や死亡への進行を改善する可能性がある。
方法: RECOVERY試験の一部として、Covid-19入院患者を1:2の比でランダムに2つのグループに分けた。第1のグループには、肺炎患者に対する通常の治療に加えて、デキサメタゾン(1日1回6mg)を最長10日間、経口の錠剤または静脈注射で投与した。第2のグループには、通常治療のみを行い、デキサメタゾンは投与しなかった。盲検化は行わなかった。研究の主要評価指標は、ランダム化から28日以内の全死因死亡率(死因を問わない死亡率)とした。
結果: 2,104 例をデキサメタゾン群,4,321 例を通常治療群に割り付けた。ランダム化から28日以内の死亡率は、デキサメタゾン群が22.9%(482/2,104例)、通常治療群が25.7%(1,110/4,321例)だった。死亡率比(デキサメタゾン群の死亡率 / 通常治療群の死亡率)は、0.83だった(95%信頼区間 0.75-0.93)(年齢補正あり・後述)。
デキサメタゾン群と通常治療群との死亡率の差や比は、ランダム化した時点の患者の呼吸管理の状態によって大きく異なっていた。①もっとも重症で、人工呼吸器やECMOによる侵襲的な呼吸管理を受けていた患者では、デキサメタゾン群のほうが通常治療群よりも死亡率が低かった(29.3% 対 41.4%,死亡率⽐ 0.64、95%信頼区間 0.51-0.81)。
②つぎに重症で、酸素の投与は受けていたが、人工呼吸器やECMOによる呼吸管理は受けていなかった患者でも、デキサメタゾン群のほうが通常治療群よりも死亡率が低かった(23.3% 対 26.2%、死亡率⽐ 0.82、95%信頼区間 0.72-0.94)。
③いっぽう、対象者の中ではもっとも軽症で、酸素の投与も人工呼吸器やECMOによる呼吸管理も受けていなかった患者では、デキサメタゾン群の死亡率は通常治療群より低くなかった(17.8% 対 14.0%,死亡率⽐ 1.19、95% 信頼区間 0.92-1.55)。結論: Covid-19入院患者にデキサメタゾンを投与することにより、重症で、ランダム化の時点で侵襲的な人工呼吸管理や酸素の投与を受けていた患者では、28日死亡率が低下した。しかし、より軽症で、人口呼吸管理や酸素投与を受けていなかった患者では、28日死亡率は低下しなかった。
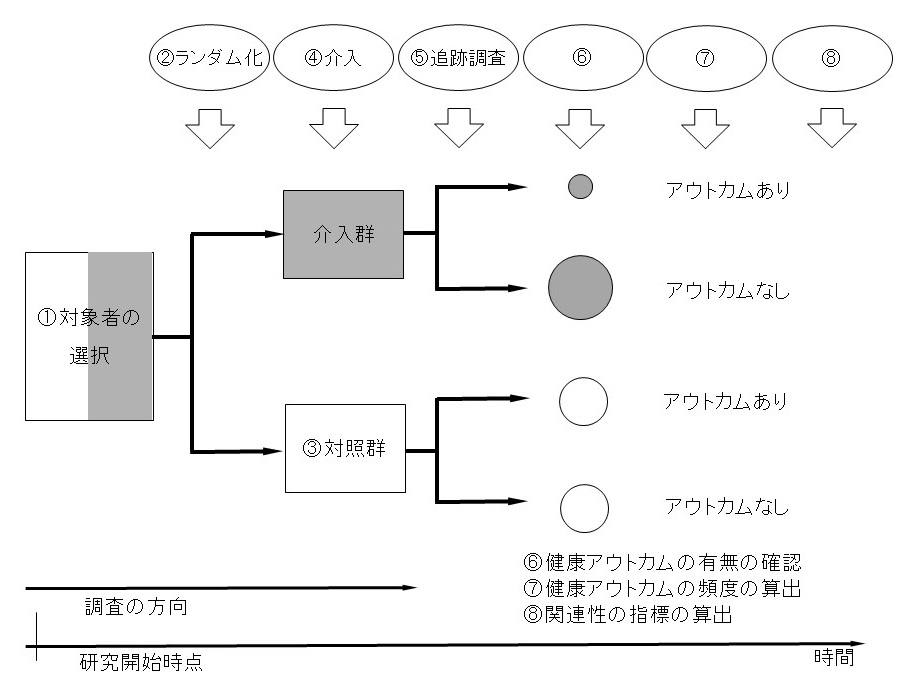
この研究は、ランダム化比較対照試験の研究デザインを採用して行われた。図表9-1にランダム化比較対照試験のシェーマを示す。図表9-2に、シェーマに基づくこの研究の調査の概略を示す。
この臨床試験が画期的だった点のひとつは、パンデミックの混乱のさなかに研究が行われたにもかかわらず、きわめて短期間で、研究の実施、研究結果の公表、診療の現場へのデキサメタゾンの導入が行われたことである。
論文著者らによると、研究計画書の第1版が作成(2020年3月13日)されてから100日も経たない期間に、対象者の登録、デキサメタゾンの投与、データ解析が行われた。2020年6月16日には、デデキサメタゾンの有効性に関する予備的な結果が、英国政府の関係機関から公表され、おなじ日に、同国のCovid-19入院患者の診療に導入された。
2020年7月17日には、論文の暫定版がNEJMにオンライン公開された。その後、英国をはじめ、欧州医学機構(European Medical Agency)、米国NIH、WHOのガイドラインが改定され、人口呼吸管理や酸素投与を受けるCovid-19入院患者に対して、デキサメタゾンの使用が標準治療として取り入れられた。
NEJM論文のオンライン公開と同時に、米国国立アレルギー・感染所研究所所長のアンソニー・ファウチ(Anthony S. Fauci)氏らが、「パンデミックの状況での研究」と題する論評を寄せている。
論説によると、かつては、疾患の集団発生(アウトブレイク)が生じている状況では、治療法などについて厳密な臨床研究を行うのはふさわしくないという考え方が一般的だった。人々が次々と死亡するような時には、可能性のあるすべての治療を試すチャンスが与えられるべきで、厳密な方法の臨床研究など行っている場合ではない、というわけだ。
しかし、学界の意見は次第に変化し、2018-2020年にコンゴ民主共和国でエボラ熱の集団発生が生じた際には、適切な規模のランダム化比較試験が行われ、2つの薬剤の有効性を明確に確認することができたという。
今回のRECOVERY試験も、こうした世界の研究動向を踏まえて行われた。Covid-19患者に対する効果的な治療法や予防法を明らかにするうえで、科学的に厳密で倫理的に適切な臨床研究は、「もっとも迅速でもっとも効率的な道すじ」(the quickest and most efficient pathway)なのであると、論評は結んでいる。
https://www.nejm.org/doi/full/10.1056/NEJMe2024638
RECOVERY試験は、研究の開始から3カ月あまりで12,000例という多数の患者を登録し、重症のCovid-19入院患者に対するデキサメタゾンの有効性を明らかにし、診療現場の実践を変えた。
大規模な臨床試験であるにもかかわらず、なぜ短期間で結果を出せたのだろうか。そこには、おもに3つの要因が寄与している。
①研究の設計や実務をできるだけシンプルにした。
②今日の情報技術を積極的に活用した。
③単一の研究計画書(プロトコル)を採用した。
順番に見ていこう。
①について、この研究のどこがシンプルなのか、いくつか例を挙げる。
第1に、研究の主要評価指標は、ランダム化してから28日以内の全死因死亡率とした。全死因死亡という評価指標の場合、死因を問わずに、患者が死亡すればアウトカムが発生したとしてカウントする。患者が死亡したか否かだけを問題にしたのだ。死亡か否かという情報であれば、集めるのは容易である。
第2に、患者の診療を行いながら研究にも参加する医療従事者の負担を軽減するために、呼吸機能、検査データなどの情報の報告を求めなかった。
第3に、患者の追跡調査に関する情報(生死、入退院、人工呼吸器の使用など)について、現場の医療従事者による報告は、ランダム化から28日後の時点(死亡や退院の場合はその時点)で、1回だけ行われた。これも通常の臨床試験であれば、追跡調査は複数回行い、くり返し情報提供を求めるのが一般的だ。しかし診療現場の担当者が、データを複数回報告するのは負担が大きい。
そこで今回は、追跡調査のデータ報告を1回のみとすることで、現場の負担を軽減した。第4に、患者の同意書、患者を臨床試験に登録する際の症例データ報告などは、1ページの簡便な様式を用いた。
②の情報技術の積極的な活用についても、例を挙げる。
第1に、現場の医療従事者が入力などに関わる情報は、診療現場でオンライン入力できるシステムを構築した。たとえば、患者を臨床試験に登録する情報をオンライン入力すると、その場でランダム化の結果が示され、患者に対して通常治療のみを行うか、通常治療に加えてデキサメタゾンを投与するかが指示された。
第2に、現場で医療従事者が入力するデータ以外の、ルーチンで収取されるデータを、最大限に活用した。具体的には、病院の電子カルテの情報(診断、処置、退院など)、患者が死亡した場合に行政が登録するデータ、病院に患者を紹介した診療所の電子カルテの情報(既往歴など)、集中治療室のデータなどだ。
フォーマットの異なる25種類のデータベースが使用されたという。2021年3月の時点で、RECOVERY試験には39,000人の対象者が登録されているが、医療従事者が手入力したデータが10万行、ルーチンのデータベースから収集されたデータは30万行に及ぶという。患者1例に対して、出所の異なる何行ものデータが存在することになる。アルゴリズムを開発し活用することで、これらのデータを整理し統合しているのだ。
https://www.thelancet.com/journals/landig/article/PIIS2589-7500(21)00063-7/fulltext
③の単一の研究計画書(プロトコル)について述べる。
臨床試験を企画する際には、「プロトコル」と呼ばれる研究計画を事前に作成する。プロトコルでは、研究の実施に必要なさまざまな項目を定義する。研究対象者の適格基準や除外基準、介入の内容(治療薬の投与量、投与方法、期間)、対照群に対する処置(プラセボを使用するかなど)、主要評価指標の定義、副次的な評価指標の定義、などである。
話はそれるが、Covid-19によるパンデミックが拡大するなか、抗マラリア薬であるヒドロキシクロロン効果を喧伝する言説が拡がった。そこで、世界の多数の研究グループが、「Covid-19患者に対するヒドロキシクロロンの有効性を評価するランダム化比較試験」のプロトコルを作成し、研究を開始した。2020年末の時点で、ヒドロキシクロロンの臨床試験が250件近く行われている。
https://www.nature.com/articles/d41586-021-01246-x
とはいえ、250件の臨床試験が、すべておなじプロトコルを採用しているわけではない。対象者の適格基準がたとえば「Covid-19の入院患者」であっても、除外基準として軽症例を除外する研究もあれば、逆に重症例を除外する研究もある。主要評価指標を「死亡率」とする研究もあれば、「重症度」の改善とする研究もあれば「入院期間」の短縮とする研究もある。ひとくちに「Covid-19入院患者に対するヒドロキシクロロンの有効性を評価するランダム化比較試験」と言っても、プロトコルが大きく異なれば、もはや別の研究と考えたほうがよい。
この場合、どのような問題が生じるか。ある研究ではヒドロキシクロロンは「有効」、別の研究では「無効」という結果が出たとしても、プロトコルが異なれば、結果を単純に比較することはできないので、解釈に困難が生じる。プロトコルの異なる臨床試験が乱立することで、ヒドロキシクロロンの意義を評価することが、かえって難しくなる。
こうした事態を改善するための対応のひとつが、単一のプロトコルを採用して、多施設の共同研究を行うことである。対象者の適格基準や除外基準、主要評価指標の定義、ランダム化の方法、データ収集の方法などについて、いわば共通のインフラを整備することだ。
RECOVOERY試験には、英国の176施設が参加した。もしもかりに、それぞれの施設の研究者が、独自のプロトコルを176件作成したら、それらの結果を単純に比較することはきわめて難しい。また、パンデミックのさなかで目の前の患者の診療に忙殺される現場の医療従事者が、施設ごとに異なるプロトコルを作成する余裕もない。176施設が単一のプロトコルを採用したことで、多数の対象者を短期間で登録することが可能になったのである。
けっきょく、RECOVERY試験は、①1980年代に心筋梗塞の治療の研究で普及した大規模でシンプルなランダム化比較対照試験という方法、②2020年代の進化した情報技術、さらに③複数の研究者が単一で共通の手順に従うプロトコル、を組み合わせることで、パンデミック下にもかかわらず大規模な臨床試験を実施し、わずか3か月で結果を出せることを実証した。臨床試験の教科書を書き換え、臨床試験の新たなスタンダードを設定したと評価されるのも理解できる。
なお、すぐ後で述べるように、RECOVERY試験では、単一のプロトコルという方法論のなかでも、とくに「マスタープロトコル」(master protocol)という方法を採用し、しかもマスタープロトコルのなかでも、「プラットフォーム試験」(platform trial)の方法を採用している。おなじランダム化比較対照試験でも、伝統的な方法から大きく飛躍した、革新的な手法を採用したのである。
https://www.nejm.org/doi/full/10.1056/NEJMoa2021436
https://www.thelancet.com/journals/landig/article/PIIS2589-7500(21)00063-7/fulltext
ランダム化比較対照試験を行う場合、これまでは、単一の疾患に対して、単一の治療法を評価する研究が多かった。しかし最近は、単一の疾患に対して複数の治療法をつぎつぎと評価したり、単一の治療法を複数の疾患に対して同時に評価したりする研究が行われるようになっている。この際に用いられるプロトコルを、とくにマスタープロトコルという。マスタープロトコルは、歴史的にはおもに抗がん剤の開発の分野で発展した方法で、つぎの3種類が代表的だ。
①アンブレラ試験(umbrella trial)。単一の疾患(たとえば肺がん)に対して、複数の薬剤の有効性や安全性を評価する。
②バスケット試験(basket trial)。単一の薬剤(たとえばがん免疫療法)の有効性や安全性を、複数の疾患(たとえば同じ遺伝子を発現している肺がん、胃がん、乳がんなど)で評価する。
③プラットフォーム試験(platform tiral)。単一の疾患に対する複数の薬剤の有効性や安全性を評価する。この際、研究の途中の段階で、評価の終わった治療薬を中止したり、新しい治療薬を追加したりすることができる。
https://www.nejm.org/doi/full/10.1056/nejmra1510062
RECOVERY試験は、これらのマスタープロトコルのなかで、プラットフォーム試験と呼ばれる研究手法を採用している。これもこの研究の革新的な点である。くわしく説明しよう。
プラットフォーム試験では、ひとつの疾患に対する複数の治療法(たとえば薬剤A、B、C)の効果を、同時に評価する。研究が進み、たとえばひとつの治療法(たとえば薬剤A)に有効性がないことがわかれば、その治療法は中止される。いっぽう、研究が開始された後に有望な治療法の候補(たとえば薬剤D)が現れれば、その治療法が追加される。
https://www.nejm.org/doi/full/10.1056/nejmra1510062
https://www.thelancet.com/journals/langlo/article/PIIS2214-109X(20)30540-4/fulltext
RECVOERY試験の当初の研究計画では、対象者を2:1:1:1の比でつぎの4グループにランダムに割り付けた。
①通常治療のみの対照群。
②通常治療+デキサメタゾン群。
③通常治療+ロピナビル・リトナビル合剤(抗HIV薬)。
④通常治療+インターフェロンβ(免疫抑制剤)。
今回解説したNEJM論文は、①通常治療のみの対照群と②通常治療+デキサメタゾン群の比較という、RECOVERY試験で評価している複数の薬剤のうちのひとつに焦点をあてた報告ということになる。
https://www.nejm.org/doi/suppl/10.1056/NEJMoa2021436/suppl_file/nejmoa2021436_protocol.pdf (p. 7)
冒頭の記述をくり返すが、これらの薬剤はいずれも、新型コロナウイルスの治療薬として新規に開発されたものではない。他の疾患に対する治療薬として承認され使用されている薬剤である。たとえばインフルエンザの場合、インフルエンザウイルスに対して特異的に作用するタミフルやリレンザのような薬剤が存在する。同様に、新型コロナウイルスに対しても、ウイルスに特異的に作用する薬剤を開発することがもっとも重要だ。しかし、こうした薬剤の開発には時間がかかる。そのためRECOVERY試験では、べつの疾患に対して使われてきた既存の薬剤を、Covid-19患者に転用して、その有効性や安全性を調べた。
2020年3月に開始されたRECOVERY試験は、現在も進行中である。研究開始から1年後の2021年3月時点では、13の治療群に患者が登録されている。登録されたCovid-19患者は約40,000人に及び、英国のCovid-19入院患者全体の約10%に相当する。この間に、デキサメタゾンとトシリズバム(抗IL-6抗体)の死亡率改善に対する有効性を明らかにした。いっぽう、アジスロマイシン(抗菌薬)、コルヒチン(抗炎症薬)、Covid-19回復者血清、ヒドロキシクロロン(抗マラリア薬)、ロピナビル・リトナビル合剤(抗HIV薬)には効果がないことも明らかにした。効果がないことが判明した治療法は中止しながら、さらに新しい治療法の評価を継続している。
https://www.nature.com/articles/d41573-021-00068-w
古典的なランダム化比較対照試験でも、たとえば対象者を3つのグループに割り付け、対照群に加えて、2つの治療法を同時に評価することはある。ただしこの場合、当初に計画した2つの治療法を評価するのに必要な人数の対象者が登録されてしまえば、それ以上の対象者の登録は行わない。また、2つの治療法の評価が終われば、研究も終了する。2つの治療法とは別の、3つ目の治療法を評価したければ、あらたに別のランダム化比較試験を計画して参加者を登録し、対照群と3つ目の治療法を行う介入群の2グループを設定する。新しい治療法を評価するたびに、新しいランダム化比較試験をそのつど実施するのが通例だ。
これに対してプラットフォーム試験では、たとえば最初に、対象者を3つのグループに割り付け、対照群に加えて、2つの治療法を同時に評価する。1つの治療法に効果がないとわかれば、この治療群に対する参加者の登録は中止する。いっぽう3つ目の治療法が候補として有望と判断されれば、あらたに治療群を設定し、新しい参加者を登録する。参加者の登録を継続しながら、効果のない治療法は中止し、有望な治療法の候補を追加する。
つまり、単一のランダム化比較試験という「プラットフォーム」の上で、多数の治療法の評価をつぎつぎと実施する。そのため、新しい治療法を評価するたびに、そのつど研究組織を立ち上げ、研究計画を立て、参加者の登録を行うような古典的なランダム化比較対照試験よりも、効率的に多数の治療法の評価が行えるという利点がある。
けっきょく、RECOVERY試験が、研究開始から1年足らずという短期間で、多数の薬剤の有効性の有無をつぎつぎと評価し、Covid-19入院患者の治療法の確立に対してめざましい成果を上げることが可能だったのは、このプラットフォーム試験の方法を採用した点が大きい。
デキサメタゾンのRECOVERY試験に関するNEJM論文に対して、ハーバード大学の研究者が論評を著し、研究の方法論上の問題点をいくつか指摘している。ここでは、①盲検化(blinding)が行われていない点と、②複数の治療薬を評価するにあたり単一で共通の対照群を設定している点について、論評を補って解説してみよう。
https://www.nejm.org/doi/full/10.1056/NEJMe2025674
まずは、①盲検化が行われていない点について述べる。デキサメタゾン試験では、通常治療+デキサメタゾンと通常治療のみの比較を行っているが、通常治療のみを行う患者に対して、デキサメタゾンに対応するプラセボは使われていない。そのため、患者も、患者の治療にあたる医療者も、患者が割り付けられているのが、通常治療+デキサメタゾンのグループなのか、通常治療のみのグループなのか、わかるようになっている。
つまり、二重盲検(double blind)の措置が取られていない。いっぱんに、盲検化が行われず、患者が所属するグループを医療者が知っていると、研究の評価指標を判定する際に過大評価や過小評価が生じる可能性がある。ただし、RECOVERY試験の主要評価指標は、全死因死亡、つまり死因を問わず患者が死亡したか否かである。患者が死亡したか否かを判定する際に、デキサメタゾンが使用されていたか否かを医療者が知っていることが、大きな影響を与えることは考えにくい。
そのいっぽう、副次的な評価指標として、退院までの日数(入院期間)と、ランダム化された時点で人工呼吸器を装着されていなかった患者が、その後に人工呼吸器の使用を開始したか死亡したかが設定されている。患者を退院させるか否かの判断や、人工呼吸器の使用を開始するかの判断は、患者を診療する医療者が行う。この医療者の判断に、患者がデキサメタゾン投与を受けているか否かを知っていることが、影響を及ぼす可能性はあるだろう。
たとえば、ある患者の状態が悪化し、人工呼吸器の使用を開始するか否かの判断に迫られた際に、この患者にはデキサメタゾンが投与されていないことを医療者が知っていれば、悪化の程度がより軽い状態でも人工呼吸器の使用を始めるかもしれない。ぎゃくに、この患者にはデキサメタゾンが投与されていることを医療者が知っていれば、しばらく経過観察を行い、人工呼吸器の使用を開始しないかもしれない。
この場合、デキサメタゾンを投与されている患者は、投与されていない患者と比べて、より重症の段階で人工呼吸器の使用が始められることになる。結果的に、人工呼吸器の使用を開始する患者の割合が、デキサメタゾン群ではじっさい以上に低くなり、薬剤の効果の過大評価につながる可能性がある。これはあくまで仮想例だが、盲検化の措置がとられず、患者がデキサメタゾンの投与を受けたか否かを医療者が知っていることで、副次的な評価指標の判定に影響を及ぼし、デキサメタゾンの効果を実際以上に過大評価したり過小評価したりする可能性は否定できない。
この研究の第2の問題点として、単一で共通の対照群を設定した問題についてはどうだろうか。
RECVOERY試験の当初の研究計画では、対象者を2:1:1:1の比で、①通常治療のみの対照群、②通常治療+デキサメタゾン群、③通常治療+ロピナビル・リトナビル合剤(抗HIV薬)群、④通常治療+インターフェロンβ(免疫抑制剤)群の4グループに分けた。つまり、②③④の3種類の介入群を評価する際に、①のグループを共通の対照群として設定した。
もしもかりに、偶然の影響を受けて、①の対照群の死亡率がたまたま非常に高かったとすれば、②③④の3種類の治療薬の有効性を、じっさい以上に過大評価する可能性がある。ぎゃくに、①の対照群の死亡率がたまたま非常に低かったとすれば、②③④の3種類の治療薬の有効性を、じっさい以上に過小評価する可能性がある。
これは、RECOVOERY試験がプラットフォーム型のランダム化比較試験の方法を採用していることに起因する問題である。古典的なランダム化比較試験の方法を採用したとすれば、②③④の3種類の介入群を評価するために、3件の臨床試験を行うことになる。この場合、②の介入群に対する対照群、③の介入群に対する対照群、④の介入群に対する対照群というように、それぞれの介入群に対して固有の対照群が3つ設定される。もしもかりに②のデキサメタゾン投与群に対する対照群の死亡率がたまたま高く、デキサメタゾンの効果を過大評価したとしても、③と④の治療群にはそれぞれ固有の対照群が設定されているため、これらの治療の効果も過大評価することにはつながらない。
複数の治療法の効果を同時に評価するために設定した、共通で単一の対照群の治療成績(死亡率)が、偶然の影響でたまたま高くなったり低くなったりして、複数の治療法の効果を、実際以上に過大評価したり過小評価したりする可能性がある。
このような「たまたま生じた偶然の影響」は、あくまで理論的に想定した仮想的な問題にすぎないと考えるかもしれない。
ところが、である。RECOVERY試験では、研究の別の部分で、まさにこの「たまたま生じた偶然の影響」が、じっさいに生じたのである。次に述べる、「ランダム化のバッドラック」の現象である。
RECOVERY試験では、登録した患者をランダムに通常治療+デキサメタゾン群(介入群)と通常治療のみ(対照群)の2グループに分けた。ランダムに2グループに分けるのは、たとえば患者ひとりずつにサイコロを振って、偶数の目が出れば介入群、奇数の目が出れば対照群に分けるのとおなじ処置である。その結果として期待されるのは、患者の特性(性別・年齢・人種・疾患の重症度など)がよく揃った2つのグループ(介入群と対照群)が作られることである。
ところがRECOVERY試験では、デキサメタゾン群の2,104人の患者の平均年齢(±標準偏差)は66.9歳(±15.4歳)、通常治療群の4,321人では65.8歳(±15.8歳)だった。つまり、デキサメタゾン群の方が通常治療群よりも、平均年齢が1.1歳高かった。
1.1歳の差というと、小さな差と感じるかもしれない。けれども筆者は、このデータをみたとき、1.1歳もの大きな差があったことに非常に驚いた。
もしもこれが、20人と40人のグループにランダムに分けた結果であれば、2つのグループの平均年齢が1歳くらい違った結果になっても、まったく驚かない。サイコロを20回振ったグループと40回振ったグループで、偶数の目が出る期待値はそれぞれ10回(10/20=0.5)と20回(20/40=0.5)だが、たとえばこれが8回(8/20=0.4)と24回(24/40=0.6)のように、期待値から多少ばらつく結果が出ても驚かないのとおなじだ。対象者の人数が10倍の200人と400人だったとしても、平均年齢に1歳くらいの差があっても、それほど驚かない。
ところが、そのさらに10倍に相当する2,104人と4,321人という大規模な集団で、ランダムに2グループに分けた結果として生じた、平均年齢の1.1歳の差は、かなり大きな差として受けとめるような話である。この規模のランダム化比較試験の場合、参加者のもっとも基本的な属性である年齢の平均値は、たとえば2つのグループで66.4歳と66.4歳のような同一の値や、66.5歳と66.3歳のように、ほぼ同一の値になることがむしろ普通である。登録した患者をランダムに2グループに分けたものの、たまたまの結果として、2群の平均年齢が揃った2群ではなく、平均年齢の異なる2群ができるという、不運=バッドラックが生じたわけである。
ランダム化が十分に成功していれば、デキサメタゾン群と通常治療群の平均年齢に差は生じず、たとえば66.4歳と66.4歳となることが期待される。いっぽう今回の研究では、デキサメタゾン群と通常治療群の平均年齢は66.9歳と65.8歳で、ランダム化のバッドラックにより1.1歳の差が生じた。
すでに起こってしまったバッドラックを、なかったことにはできない。ここで重要になるのは、2グループの平均年齢に差があることで、全体の研究結果にどの程度の影響が生じたかを、定量的に評価することである。RECOVERY試験の研究者は、じっさいにこの評価を行い、その結果を論文の追加資料に報告している。結果の一部を示して説明する。
https://www.nejm.org/doi/suppl/10.1056/NEJMoa2021436/suppl_file/nejmoa2021436_appendix.pdf (p. 33)
図表9-3には、「死亡率比」、すなわち「死亡率」の「比」が示されている。「死亡率比」の分子は、デキサメタゾン群+通常治療群(介入群)の死亡率。分母は、通常治療のみの群(対照群)の死亡率である。介入群の死亡率(分子)が、対照群の死亡率(分母)より小さければ、死亡率比は1より小さくなる。死亡率比が1より小さくなるほど、対照群と比べて介入群の死亡率は小さく、介入の効果(デキサメタゾン投与の効果)が大きいことを意味する。
「死亡率比」には、「年齢補正なし(0.87)」と「年齢補正あり(0.83)」の2つの数値が示されている。「年齢補正なし」の死亡率比は、介入群と対照群の平均年齢に1.1歳の差がある(2群の年齢分布に差がある)状態のままで計算した結果である。この死亡率比は0.87で、対照群の死亡率(分母)と比べて介入群の死亡率(分子)は0.87倍と低かった。1-0.87=0.13なので、別の表現をすると、介入群の死亡率は対照群の死亡率よりも13%低かった。デキサメタゾン投与により、患者の死亡率が13%低下したことを示す結果だった。
「年齢補正あり」の死亡率比も示されている。介入群と対照群の平均年齢に実際には1.1歳の差があるものの、統計的な手法を使って、かりに2群の平均年齢に差がなかった(年齢分布に差がなかった)場合に想定される死亡率比を計算している。じっさいには、ランダム化のバッドラックにより2群の年齢の偏りが生じてしまったが、もしもかりに、ランダム化が成功して2群の年齢分布が揃い、偏りが生じなかった場合に想定される死亡率を算出していることになる。
この「年齢補正あり」の死亡率は0.83だった。つまり、対照群の死亡率と比べて介入群の死亡率は0.83倍と低かった。1-0.83=0.17なので、別の表現をすると、介入群の死亡率は対照群の死亡率よりも17%低く、デキサメタゾン投与により、患者の死亡率が17%低下したことを示す結果だった。
2つの死亡率比をあらためて比べると、「年齢補正なし」では0.87、「年齢補正あり」では0.83。デキサメタゾン投与による死亡率の低下は、「年齢補正なし」の死亡率比で見ると13%だが、「年齢補正あり」の死亡率比で見ると17%となる。デキサメタゾンが死亡率を下げる効果は、「年齢補正なし」の13%よりも「年齢補正あり」の17%の方が大きい。4%の差は、けっして小さな違いではない。
どちらの結果を採用するのが適切だろうか。
RECOVERY試験の研究者がメインの結果として採用しているのは、2群の平均年齢が1.1歳異なるという実際のデータからそのまま計算される、「年齢補正なし」の死亡率比(0.87倍、13%低下)ではない。実際のデータに統計的な操作を加えて、2群の平均年齢に差がない場合を想定して算出した、「年齢補正あり」の死亡率比(0.83倍、17%低下)のほうである。つまり、ランダム化のバッドラックにより2群の年齢分布に偏りが生じてしまったが、偏りが生じなかった場合に想定されるデータを、メインの結果として採用し報告しているのである。
「年齢補正あり」の結果のほうが、「年齢補正なし」の結果よりも適切なのはなぜだろうか。以下、その次第を述べる。介入群の平均年齢は、対照群の平均年齢よりも、1.1歳高い。いっぱんに、Covid-19入院患者の死亡率は、年齢が高いほうが、年齢が低い場合より、高い傾向がある。RECOVERY試験の介入群は、対照群よりも年齢が高いので、デキサメタゾンの投与の有無にかかわらず、死亡リスクが最初から高い状態にあると想定される。
もともと年齢が高く死亡リスクも高い介入群の患者にデキサメタゾンを投与し、年齢補正をせずに算出すると、介入群の死亡率は対照群より13%低いという結果だった。これに対して、年齢補正を行い、2群の年齢に偏りがなく、年齢によるもともとの死亡リスクを統計的にそろえた状態を想定すると、死亡率の低下は17%と、より大きくなった。
つまり、年齢補正を行わない13%の死亡率低下というデータは、デキサメタゾンのじっさいの効果を過小評価しており、年齢補正を行って算出された17%の死亡率低下というデータのほうが、ほんらいのデキサメタゾンの効果を示すうえで適切である。こうした理由から、RECOVERY試験の研究者は、年齢補正を行った死亡率比を、メインの結果として採用し報告している。
RECOVERY試験は、Covid-19の第1波の混乱のさなかで英国の現場の医療者が協力して実施した、大規模なランダム化比較対照試験である。仮説や研究プロセスをシンプルにし、情報技術を積極的に活用することで、患者の診療に追われる現場の医療者が参加しやすくした。研究開始からわずか3か月で、デキサメタゾンが呼吸補助を必要とする入院患者の死亡率の改善に有効であることを明らかにした。
くわえて、プラットフォーム臨床試験という革新的な研究手法を用いることで、デキサメタゾンの有効性のほか、ヒドロキシクロロンや回復患者の血清投与が無効であることなど、複数の治療の意義をつぎつぎと明らかにした。臨床試験の教科書を書き換えるであろう革新的なこの研究は現在も進行中で、新しい治療の評価が続けられ、その結果は世界の診療現場や診療ガイドラインに反映されている。
とはいえ、デキサメタゾンのRECOVERY試験にも、限界や問題点はある。デキサメタゾンに対するプラセボを使わず、二重盲検の措置も取られていない。登録した患者をランダムにデキサメタゾン群と通常治療群に分けたはずが、ランダム化のバッドラックが生じ、結果的に患者の平均年齢が異なってしまい、研究当初には予定していなかった年齢補正の解析を行わざるをえなかった。
筆者自身がもっとも革新的と感じるのは、どの治療薬や治療法がCovid-19患者に有効なのか皆目見当がつかないパンデミックの混乱の初期に、このランダム化比較対照試験がすばやく計画され実行された点である。「なにが有効かわからないなかで、悠長にランダム化比較対照試験などを行っている場合ではない。とりあえず可能性のある治療法はなんでも試してみることが必要であり、倫理的でさえある」という類の議論に抗して、「なにが有効かわからないからこそ、ランダム化比較対照試験で評価することが科学的であり倫理的でもあり、しかもそれが実行可能である」ことを、RECOVOERY試験は事実によって示したのである。
パンデミックの時だからこそ、エクスキューズをせずに、緊急性と科学性を両立させるための正面突破を行った。その結果、世界のどこの病院にもあるありふれた薬剤であるデキサメタゾンにより、呼吸補助が必要な入院患者の死亡率を改善することを示した。RECOVOERY試験のこの結果は、公表後すぐに世界の臨床医に共有され、無数のCovid-19患者の生命を救い、今日も救い続けている。
この偉大な成果から、学ぶことは少なくないだろう。
特効薬となる新しい新型コロナウイルス薬はまだありませんが、すでに使われてきた各種の薬の有効性が多方面で検討されてきました。前回紹介したイベルメクチンは有効性が確認されず、そもそもその論文は撤回されていましたが、今回取り上げた薬をはじめいろいろな研究は今も続いています。ワクチンや治療薬など、そうした研究を公表する疫学論文を具体的に読んでいくことも、おなじように続けていくことが大事です。疫学理論の解説とその読み方を、坪野吉孝さんに単行本としてまとめていただく予定です。この連載はいったんお休みになりますが、刊行までいましばらくお待ちください。[編集部]
》》》バックナンバー
第1回 感染と情報の爆発
第2回 パンデミックの転換点を、300語で読む――ファイザー社ワクチンのランダム化比較対照試験①
第3回 「重症化」予防がワクチンの目的か︖――ファイザー社ワクチンのランダム化比較対照試験②
第4回 ランダム化比較対照試験の理論――ランダム化・バッドラック・エクイポイズ
第5回 リアルワールドエビデンスの「マジック」――ファイザー社ワクチンの後向きコホート研究
第6回 Covid-19ワクチンによる「発症」予防と「感染」予防――ファイザー社とモデルナ社のmRNAワクチンの前向きコホート研究
第7回 急速に蔓延する変異株と、どうたたかうか――デルタ株に対するファイザー社ワクチンの症例対照研究
第8回 コロナ時代の最初の巨大な研究スキャンダル――血圧降下薬・ヒドロキシクロロキン・イベルメクチンの死亡リスクの後向きコホート研究
第9回 パンデミックの時こそ、緊急性と科学性を両立させる――デキサメタゾンのランダム化比較対照試験